02-02-2023 06:27 Химия
В прошлом посте я как-то начал путаться. Нуневажно, идем далее.
Пошли по видам связей между атомами. Самая очевидная - ковалентная. То есть связь при которой один и тот же электрон используется одновременно несколькими атомами. В идеале создает завершенная орбиталь. Такая орбиталь называется уже не атомной а молекулярной, т.к. принадлежит всей молекуле.
Самая простая химическая реакция это H + H = H2. Два водорода, каждый из которых имеет по заполненной наполовину первой орбитали, объединяются в молекулу с единственной полностью заполненной двумя электронами орбиталью.
В случае с известной формулой воды H2O - эти два электрона от обоих водородов вставляет в свою незаконченную орбиталь кислород, которому самому не хватает двух электронов до фулхауса.
Если орбиталь у атома-молекулы завершена - в нем меньше энергии, чем в атоме с незавершенной, то есть при объединении незавершенных орбиталей в завершенную происходит выделение энергии. Собственно на выделение ее при реакции водорода с кислородом - основана базовая идея водородного ракетного двигателя.
Ковалентная связь происходит только между парами электронов. Либо два атома с нечетным количеством электронов, если им не хватает обоим по одному до фулхауса - меняются между собой одним финальным электроном (как в случае с водородом). Либо выдается два электрона тому, кому они нужны (как в случае с реакцией двух водородов с кислородом). Больше двух электронов (в ковалентной связи) в общее пользование не выдается, т.к. между атомами нет столько места.
Ионная связь - когда один атом отрывает электроны у другого. В результате один получает заполненную оболочку, а второй становится ионом.
Отдавший электрон атом отмечается плюсом. К примеру в реакции натрия с фтором, первый отдает электрон и записывается как Na+, получивший же лишний электрон фтор записывается как F-. Я так понимаю, что между ними возможна и ковалентная связь, где они опять же возьмут этот электрон в общее пользование и оба таким образом закроют пасьянс.
Ковалентная связь может быть полярной. К примеру когда два водорода обменялись электронами с кислородом в молекуле воды H2O по идее никто ничего не получил и не потерял. Однако кислород сильнее "хочет" завершить свою оболочку чем водород. Они сильнее притягивает к себе чужие электроны. Тянет одеяло на себя. В результате атом водорода хотя и не потерял электрон, однако этот электрон у него "оттянули", и хотя совсем водород и не стал ионом - чуть-чуть стал. Небольшой плюс атомы водорода все-таки получают, а кислород - небольшой минус.
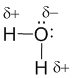
В любой связи разных элементов - всегда кто-то тянет сильнее а кто-то слабее, то есть такая связь всегда полярная. Наоборот если связаны одинаковые атомы - они тянут друг друга с одинаковой силой.
И вот теперь валентность. Фактически валентность означает сколько электронов атом готов отдать или принять. Валентностей у атома обычно несколько. Он может сколько-то атомов отдать или сколько-то принять в общее пользование причем разные количества, в зависимости от того сколько заполненных оболочек он готов получить или потерять. Однако среди валентностей всегда есть главная (иногда несколько главных) обозначающая сколько он готов отдать-получить с наибольшей силой.
Есть подробная вариация таблицы Менделеева, где валентности написаны под атомными весами-номерами, при этом главные выделены жирным шрифтом.
Странным образом эта таблица на белорусском языке, а таблицы с валентностями на русском я не нашел. У нас почему-то вот не любят валентность указывать и хоть ты тресни.
Положительное число означает сколько электронов атом готов отдать. Отрицательное - сколько принять.
Общие для разных атомов электроны называются валентными. Почему-то каждый общий электрон называют "валентной парой" при том что по факту он один, это атомов два, вокруг которых он вертится.
Собственно на этом я ответил на свой изначальный вопрос к химии - по какой логике вещества реагируют. Вот по этой и реагируют. Пытаются заполнить орбитали - и для этого реагируют.
Так-то у меня больше вопросов к химии нет. Но раз уж начал, пошли дальше.
Молекулы могут образовывать бесконечное "полотно" из связей. Это называется кристаллической решеткой, и тогда записать формулу целиком нереально. К примеру формула кварца это SiO2, но по факту это бесконечная лента кремниев и кислородов. Кремний связан с двумя кислородами слева и двумя справа, каждый из кислородов с одним кремнием слева и одним справа, получается SiO2SiO2SiO2SiO2SiO2 и так далее.
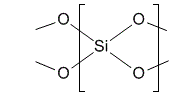
Возврат к полярности - обычно сильнее к себе тянут электроны вещества которые выше в таблице Менделеева так как они тянут электроны на более низкие орбиты, и чем ниже орбита тем больше притяжение ядра. Однако водород, судя по всему, исключение. Хотя это и первый элемент, то есть по идее у него единственного все происходит на первом этаже ближе всех к ядру и связь должна быть самая сильная. Однако странным образом именно водород не тянет.
Судя по всему это зависит еще от массы - у водорода она крайне низкая и равна почти единице, тот же кислород в 16 раз тяжелее. Обычно разница между массой элементов не такая большая, но в случае конкретно с водородом она огромная. А у кого больше масса тот сильнее тянет.
Сильнее всех элементов тянет фтор, он в любой вообще связи получает отрицательный заряд. Он тянет так сильно, что эта связь уже считай ионная. То есть он делает ионами атомы с которыми связан, при том что они даже не лишились своих электронов, но почти-почти лишились.
При ионной связи, хотя у атома и отодрали часть электронов - жертва продолжает летать рядом с агрессором, потому что у них разные заряды и поэтому они притягиваются друг к другу, хотя общих электронов у них и нет. То есть все равно образовывается общая молекула.
Да кстати относительно масс - меня вот всегда заебывало, что в химии все принято считать в молях. При том что моль - это относительная масса. Ну то есть ничего не мешает тебе взять любую вообще другую массу в мире вместо моля - к примеру граммы, килограммы, тонны. И все будет работать ровно точно так же, все формулы, все соотношения. Но нет, химикам обязательно надо было выебнуться, и поэтому никаких граммов. Моли.
Далее про связи. Заряд - важная часть электропроводности. Поэтому ионные соединения обычно хорошо проводят электричество, то есть чем меньше разница в притяжении между атомами молекулы - тем меньший заряд они получают - и тем хуже молекула проводит электричество. Чистые вещества с завершенными электронными орбиталями - либо вообще не проводят ток, либо почти его не проводят. Тут бы на самом деле им рассказать вообще о химическом смысле электричества, но этот момент авторы пропускают и зря.
Чем сильнее ядро притягивает к себе электроны - тем более электроотрицателен атом - тем хуже через него проходит электричество потому что нужно больше энергии, чтобы выбить его электроны, а именно движущиеся между атомами электроны это электричество и есть.
Далее глава про форму молекул. Это мне вообще не интересно.
Другое название отдачи электронов атома - окисление. Соответственно чем больше электронов атом отдал - тем больше его степень окисления. Если атом получил лишние электроны - его степень окисления отрицательная. Так же, если электрон оттянут у ядра частично - его степень окисления меньше единицы. Фактически она равна условной силе заряда.
Далее описание кристаллических решеток. Это я знаю.
Далее описание таблицы Менделеева. А, валентность чаще всего соответствует номеру столбца. Этого я не заметил. У шестого столбца валентность обычно -2, у седьмого -1, восьмой срал на всех.
У каждого столбца есть отдельное название:
1 - щелочные металлы (кроме водорода)
2 - щелочноземельные металлы
3,4,5 - без названия
6 - халькогены
7 - галогены
8 - благородные газы
Существует два вида таблицы Менделеева - длинная и короткая. В короткой 8 столбцов, а в длинной 17. В мире распространена длинная, а в России в основном короткая.
Отдельно под таблицей выносятся латиноиды (редкоземельные элементы) и актиноиды - это элементы шестого и седьмого "этажей", где находятся особо большие семиклеточные орбитали. По идее на восьмом этаже должны быть еще более огромные орбитали, но элементы восьмого этажа наука еще не синтезировала, там огромная энергия для этого нужна, чтобы понапихать в ядро требуемое количество массы. Плюс оно тут же начнет разваливаться (собственно разваливается - читай радиоактивен - уже шестой этаж под конец), так что непонятно зачем этим заниматься.
Общие принципы, идущие через всю таблицу.
Химические реакции отличаются от ядерных тем, что в химических изменения происходят только с электронами, а с ядрами ничего не происходит. В ядерных, очевидно, происходит.
Таким образом в химии не важно что ты делаешь с веществом - после всех преобразований в нем останется ровно столько же ядер тех же элементов, что было изначально.
Собственно, учитывая что в природе, как минимум в пределах Земли, вообще с ядерными реакциями не густо - состав материалов практически не меняется, просто они перемешиваются в разных комбинациях.
Далее типы химических реакций.
Реакция соединения - из нескольких веществ получилось одно, безотходно.
Разложения - из одного вещества получилось несколько.
Реакция обмена - вещества обменялись атомами.
Реакция замещения - атом встроился в вещество и одновременно выкинул из него другой атом.
Далее закон сохранения массы - знаю.
Изотермические и эндотермические - знаю.
Молярная масса - знаю.
Молярный объем, закон/постоянная авогадро - знаю.
Связь между массой, температурой, объемом, давлением - вээ, ну скажем так, принцип понимаю.
Вычисления веса элементов для правильной реакции - знаю.
Высчитывания веса элементов для реакций обмена, где надо чтобы верное количество поглощалось и выделялось - принцип понимаю.
Далее главы, посвященные отдельным элементам. Ой я всего этого страшно начитался когда-то. Это опять биология под видом химии.
Соединения элементов с кислородом - оксиды.
Глава про озон и озоновый слой, нет спасибо.
Глава про водород. Глава про воду.
Глава про растворы, насыщенность, концентрация, хлориды, сульфаты прочее прочее. Биология снова.
Классы соединений - оксиды, кислоты, основания, соли. Это наверное может быть интересно, но как-нибудь в другой раз.
Индикаторы. Знаю.
Классы неорганических соединений.
Термохимия. Опять же базовую идею понимаю, а углубляться непонятно зачем.
Скорость реакций. Ок.
Гомогенные и гетерогенные реакции - фактически означает в один прием реакция идет или хуй знает как.
Катализ - искусственное ускорение или замедление реакции. Ок.
Химическое равновесие. Ну это когда никто ни с кем не реагирует. Дальше.
Электролиты - вещества которые распадаются на ионы. И соответственно реакции такого распада.
Нейтральные, кислые и щелочные растворы. Ок.
И все, на этом курс с сайта закончен. Там как минимум еще есть органическая химия. Я помню с ней у меня в школе кстати проблем не было. Я на следующем витке пересмотрю.
А на сейчас хватит. Я сделаю еще паузу и пройдусь по еще одному пробелу в своем образовании - электронике.
Пошли по видам связей между атомами. Самая очевидная - ковалентная. То есть связь при которой один и тот же электрон используется одновременно несколькими атомами. В идеале создает завершенная орбиталь. Такая орбиталь называется уже не атомной а молекулярной, т.к. принадлежит всей молекуле.
Самая простая химическая реакция это H + H = H2. Два водорода, каждый из которых имеет по заполненной наполовину первой орбитали, объединяются в молекулу с единственной полностью заполненной двумя электронами орбиталью.
В случае с известной формулой воды H2O - эти два электрона от обоих водородов вставляет в свою незаконченную орбиталь кислород, которому самому не хватает двух электронов до фулхауса.
Если орбиталь у атома-молекулы завершена - в нем меньше энергии, чем в атоме с незавершенной, то есть при объединении незавершенных орбиталей в завершенную происходит выделение энергии. Собственно на выделение ее при реакции водорода с кислородом - основана базовая идея водородного ракетного двигателя.
Ковалентная связь происходит только между парами электронов. Либо два атома с нечетным количеством электронов, если им не хватает обоим по одному до фулхауса - меняются между собой одним финальным электроном (как в случае с водородом). Либо выдается два электрона тому, кому они нужны (как в случае с реакцией двух водородов с кислородом). Больше двух электронов (в ковалентной связи) в общее пользование не выдается, т.к. между атомами нет столько места.
Ионная связь - когда один атом отрывает электроны у другого. В результате один получает заполненную оболочку, а второй становится ионом.
Отдавший электрон атом отмечается плюсом. К примеру в реакции натрия с фтором, первый отдает электрон и записывается как Na+, получивший же лишний электрон фтор записывается как F-. Я так понимаю, что между ними возможна и ковалентная связь, где они опять же возьмут этот электрон в общее пользование и оба таким образом закроют пасьянс.
Ковалентная связь может быть полярной. К примеру когда два водорода обменялись электронами с кислородом в молекуле воды H2O по идее никто ничего не получил и не потерял. Однако кислород сильнее "хочет" завершить свою оболочку чем водород. Они сильнее притягивает к себе чужие электроны. Тянет одеяло на себя. В результате атом водорода хотя и не потерял электрон, однако этот электрон у него "оттянули", и хотя совсем водород и не стал ионом - чуть-чуть стал. Небольшой плюс атомы водорода все-таки получают, а кислород - небольшой минус.

В любой связи разных элементов - всегда кто-то тянет сильнее а кто-то слабее, то есть такая связь всегда полярная. Наоборот если связаны одинаковые атомы - они тянут друг друга с одинаковой силой.
И вот теперь валентность. Фактически валентность означает сколько электронов атом готов отдать или принять. Валентностей у атома обычно несколько. Он может сколько-то атомов отдать или сколько-то принять в общее пользование причем разные количества, в зависимости от того сколько заполненных оболочек он готов получить или потерять. Однако среди валентностей всегда есть главная (иногда несколько главных) обозначающая сколько он готов отдать-получить с наибольшей силой.
Есть подробная вариация таблицы Менделеева, где валентности написаны под атомными весами-номерами, при этом главные выделены жирным шрифтом.
Странным образом эта таблица на белорусском языке, а таблицы с валентностями на русском я не нашел. У нас почему-то вот не любят валентность указывать и хоть ты тресни.
Положительное число означает сколько электронов атом готов отдать. Отрицательное - сколько принять.
Общие для разных атомов электроны называются валентными. Почему-то каждый общий электрон называют "валентной парой" при том что по факту он один, это атомов два, вокруг которых он вертится.
Собственно на этом я ответил на свой изначальный вопрос к химии - по какой логике вещества реагируют. Вот по этой и реагируют. Пытаются заполнить орбитали - и для этого реагируют.
Так-то у меня больше вопросов к химии нет. Но раз уж начал, пошли дальше.
Молекулы могут образовывать бесконечное "полотно" из связей. Это называется кристаллической решеткой, и тогда записать формулу целиком нереально. К примеру формула кварца это SiO2, но по факту это бесконечная лента кремниев и кислородов. Кремний связан с двумя кислородами слева и двумя справа, каждый из кислородов с одним кремнием слева и одним справа, получается SiO2SiO2SiO2SiO2SiO2 и так далее.

Возврат к полярности - обычно сильнее к себе тянут электроны вещества которые выше в таблице Менделеева так как они тянут электроны на более низкие орбиты, и чем ниже орбита тем больше притяжение ядра. Однако водород, судя по всему, исключение. Хотя это и первый элемент, то есть по идее у него единственного все происходит на первом этаже ближе всех к ядру и связь должна быть самая сильная. Однако странным образом именно водород не тянет.
Судя по всему это зависит еще от массы - у водорода она крайне низкая и равна почти единице, тот же кислород в 16 раз тяжелее. Обычно разница между массой элементов не такая большая, но в случае конкретно с водородом она огромная. А у кого больше масса тот сильнее тянет.
Сильнее всех элементов тянет фтор, он в любой вообще связи получает отрицательный заряд. Он тянет так сильно, что эта связь уже считай ионная. То есть он делает ионами атомы с которыми связан, при том что они даже не лишились своих электронов, но почти-почти лишились.
При ионной связи, хотя у атома и отодрали часть электронов - жертва продолжает летать рядом с агрессором, потому что у них разные заряды и поэтому они притягиваются друг к другу, хотя общих электронов у них и нет. То есть все равно образовывается общая молекула.
Да кстати относительно масс - меня вот всегда заебывало, что в химии все принято считать в молях. При том что моль - это относительная масса. Ну то есть ничего не мешает тебе взять любую вообще другую массу в мире вместо моля - к примеру граммы, килограммы, тонны. И все будет работать ровно точно так же, все формулы, все соотношения. Но нет, химикам обязательно надо было выебнуться, и поэтому никаких граммов. Моли.
Далее про связи. Заряд - важная часть электропроводности. Поэтому ионные соединения обычно хорошо проводят электричество, то есть чем меньше разница в притяжении между атомами молекулы - тем меньший заряд они получают - и тем хуже молекула проводит электричество. Чистые вещества с завершенными электронными орбиталями - либо вообще не проводят ток, либо почти его не проводят. Тут бы на самом деле им рассказать вообще о химическом смысле электричества, но этот момент авторы пропускают и зря.
Чем сильнее ядро притягивает к себе электроны - тем более электроотрицателен атом - тем хуже через него проходит электричество потому что нужно больше энергии, чтобы выбить его электроны, а именно движущиеся между атомами электроны это электричество и есть.
Далее глава про форму молекул. Это мне вообще не интересно.
Другое название отдачи электронов атома - окисление. Соответственно чем больше электронов атом отдал - тем больше его степень окисления. Если атом получил лишние электроны - его степень окисления отрицательная. Так же, если электрон оттянут у ядра частично - его степень окисления меньше единицы. Фактически она равна условной силе заряда.
Далее описание кристаллических решеток. Это я знаю.
Далее описание таблицы Менделеева. А, валентность чаще всего соответствует номеру столбца. Этого я не заметил. У шестого столбца валентность обычно -2, у седьмого -1, восьмой срал на всех.
У каждого столбца есть отдельное название:
1 - щелочные металлы (кроме водорода)
2 - щелочноземельные металлы
3,4,5 - без названия
6 - халькогены
7 - галогены
8 - благородные газы
Существует два вида таблицы Менделеева - длинная и короткая. В короткой 8 столбцов, а в длинной 17. В мире распространена длинная, а в России в основном короткая.
Отдельно под таблицей выносятся латиноиды (редкоземельные элементы) и актиноиды - это элементы шестого и седьмого "этажей", где находятся особо большие семиклеточные орбитали. По идее на восьмом этаже должны быть еще более огромные орбитали, но элементы восьмого этажа наука еще не синтезировала, там огромная энергия для этого нужна, чтобы понапихать в ядро требуемое количество массы. Плюс оно тут же начнет разваливаться (собственно разваливается - читай радиоактивен - уже шестой этаж под конец), так что непонятно зачем этим заниматься.
Общие принципы, идущие через всю таблицу.
Химические реакции отличаются от ядерных тем, что в химических изменения происходят только с электронами, а с ядрами ничего не происходит. В ядерных, очевидно, происходит.
Таким образом в химии не важно что ты делаешь с веществом - после всех преобразований в нем останется ровно столько же ядер тех же элементов, что было изначально.
Собственно, учитывая что в природе, как минимум в пределах Земли, вообще с ядерными реакциями не густо - состав материалов практически не меняется, просто они перемешиваются в разных комбинациях.
Далее типы химических реакций.
Реакция соединения - из нескольких веществ получилось одно, безотходно.
Разложения - из одного вещества получилось несколько.
Реакция обмена - вещества обменялись атомами.
Реакция замещения - атом встроился в вещество и одновременно выкинул из него другой атом.
Далее закон сохранения массы - знаю.
Изотермические и эндотермические - знаю.
Молярная масса - знаю.
Молярный объем, закон/постоянная авогадро - знаю.
Связь между массой, температурой, объемом, давлением - вээ, ну скажем так, принцип понимаю.
Вычисления веса элементов для правильной реакции - знаю.
Высчитывания веса элементов для реакций обмена, где надо чтобы верное количество поглощалось и выделялось - принцип понимаю.
Далее главы, посвященные отдельным элементам. Ой я всего этого страшно начитался когда-то. Это опять биология под видом химии.
Соединения элементов с кислородом - оксиды.
Глава про озон и озоновый слой, нет спасибо.
Глава про водород. Глава про воду.
Глава про растворы, насыщенность, концентрация, хлориды, сульфаты прочее прочее. Биология снова.
Классы соединений - оксиды, кислоты, основания, соли. Это наверное может быть интересно, но как-нибудь в другой раз.
Индикаторы. Знаю.
Классы неорганических соединений.
Термохимия. Опять же базовую идею понимаю, а углубляться непонятно зачем.
Скорость реакций. Ок.
Гомогенные и гетерогенные реакции - фактически означает в один прием реакция идет или хуй знает как.
Катализ - искусственное ускорение или замедление реакции. Ок.
Химическое равновесие. Ну это когда никто ни с кем не реагирует. Дальше.
Электролиты - вещества которые распадаются на ионы. И соответственно реакции такого распада.
Нейтральные, кислые и щелочные растворы. Ок.
И все, на этом курс с сайта закончен. Там как минимум еще есть органическая химия. Я помню с ней у меня в школе кстати проблем не было. Я на следующем витке пересмотрю.
А на сейчас хватит. Я сделаю еще паузу и пройдусь по еще одному пробелу в своем образовании - электронике.
[ case study ]
Комментарии:
Подведу итоги года
[Print]
Marta